Ete là gì? Ete có công thức và tính chất vật lí là gì? tính chất hóa học của este như thế nào? Để giải đáp thắc mắc đó Kovacova sẽ gửi đến bạn chi tiết về định nghĩa cũng như tính chất và ứng dụng quan trọng của chúng.
Tính chất hóa học của ete [Đầy đủ nhất]
Khái niệm về ete
Ete (ête) là tên gọi chung cho tập hợp những hợp chất hữu cơ có chứa nhóm chức ête – nguyên tử oxy liên kết cùng hai nhóm ankyl.
Ví dụ: êthôxyêtan(thuốc gây mê dietyl ête) , CH3-CH2-O-CH2-CH3 hay dung môi
Ete hóa là quá trình tạo ete từ ancol.
Ví dụ: phản ứng tạo đietyl ete:
2C2H5OH → C2H5-O-C2H5 + H2O (có xúc tác H2SO4, ở 140 độ C)
Công thức của ete
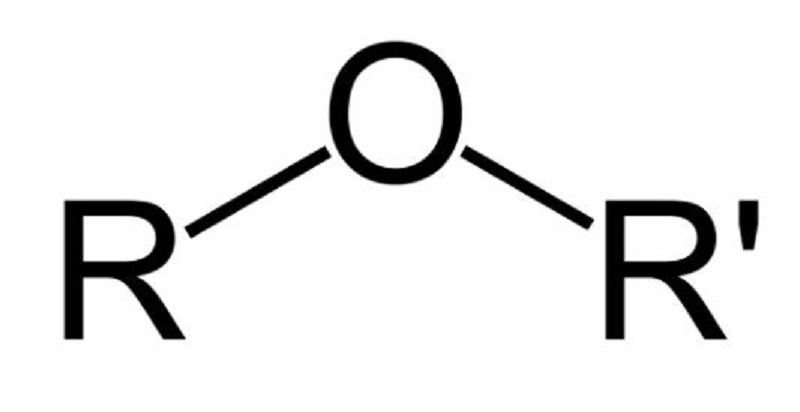
Ete công thức là R-O-R’. Tuy nhiên, không phải ở mọi hợp chất có công thức này đều là các ete. Một số lớp hợp chất hữu cơ cũng có cùng công thức tổng quát R-O-R’:
- Những hợp chất vòng thơm như furan trong đó có nguyên tử oxi là một phần của vòng thơm
- Các hợp chất mà trong đó có một trong số các nguyên tử cacbon tiếp ngay sau nguyên tử oxi sẽ được liên kết với oxi, nitơ hay lưu huỳnh.
- Các este R-C(=O)-O-R
- Các axetat: R-CH-O-R)-O-R
- Các aminal: R-CH(-NH-R)-O-R
- Các anhydrit R-C(=O)-O-C(=O)-R
Tính chất vật lý của ete
- Các phân tử ete không thể tạo ra những liên kết hiđro với nhau, từ đó cho kết quả là chúng có điểm sôi tương đối thấp khi so sánh cùng các loại ancol tương tự
- Chúng không ưa nước nhiều so với este hay amit có cấu trúc tương tự
Tính chất hóa học của ete
- Ete là những hợp chất có phản ứng hóa học rất kém. Chúng chỉ bị phân hủy trong điều kiện rất mạnh như đốt nóng cùng BF3 hoặc đun sôi trong HBr. Có thể chia cắt các ete bằng axit vô cơ chứa halogen thấp phân tử khác chẳng hạn như HCl nhưng quá trình diễn ra rất chậm. Chỉ có HBr và HI có thể chia cắt chúng với tốc độ nhận thấy được.
- Chúng có thể phản ứng như là các bazơ Lewis
- Đối với các epoxit hay các ete vòng trong các vòng ba thành viên rất dễ bị tổn thương bởi các tấn công kiểu ái lực hạt nhân(nucleophil).
- Với những ete bậc nhất, bậc hai có nhóm OH ngay sau nguyên tử oxy của ete dễ dàng tạo thành các epoxit hữu cơ có khả năng gây nổ cao khi có mặt của oxy, ánh sáng, kim loại và các tạp chất aldehit. Do vậy, các ette như dietyl ete và THF thường không sử dụng để làm dung môi trong các quy trình công nghiệp.
Một số loại ete quan trọng
- etylen oxit: loại ete vòng nhỏ nhất
- Đimetyl ete: chất đẩy trong bình xịt
- Đietyl ete: loại dung môi thông dụng với điểm sôi thấp
- Đioxan: loại ete vòng với điểm sôi cao
- THF: ete vòng, một trong những ête phân cực đơn giản nhất được dùng làm dung môi
- Anisol: là thành phần chính trong tinh dầu hồi
- Các ête vòng hoa: được dùng như các chất xúc tác chuyển pha.
Ứng dụng của ete

Mỗi loại ete lại mang đến những công dụng khác nhau và được suwr dungj rộng rãi trong nhiều lĩnh vực như diethyl ether,…
– Diethyl Ether hay ete ethyl là một hợp chất hữu cơ với công thức hóa học (C2H5)2O, thường được sử dụng dưới dạng dung môi và chủ yếu dùng trong làm thuốc gây mê mang đến hiệu quả cao. Đây là dung môi quan trọng cho nhiều ứng dụng khác nhau trong nhiều ngành nghề như là:
- Trong y tế: được dùng trong việc gây mê. Nó được sử dụng để khởi mê và gây mê, duy trì mê trong suốt quá trình phẫu thuật thông qua đường hô hấp. Tuy nhiên, việc sử dụng hợp chất này có thể dẫn đến vài tác dụng phụ không mong muốn sau phẫu thuật như là buồn nôn, nôn, khó thở,… Vì vậy, nó đã được thay thế bằng các loại thuốc gây mê khác
- Trong phòng thí nghiệm: là một trong các dung môi được sử dụng khá quen thuộc trong phòng thí nghiệm. Do khả năng hòa tan trong nước kém (chỉ 6,9 g/100ml) và trong điều kiện nước 25 độ C là 1,5 g/100ml, nó được dùng để phản ứng với Grignard và nhiều loại phản ứng khác
- Trong sản xuất công nghiệp: sử dụng để làm nhiên liệu, dùng làm động cơ đánh lửa theo mô hình carbureted nén. Ngoài ra, diethyl ether có số cetane cao 85 – 96 được sử dụng trong làm chất lỏng khởi đầu, kết hợp cùng các sản phẩm chưng cất dầu mỡ cho động cơ xăng và diesel nhờ vào độ bay hơi cao và điểm chớp cháy thấp. Một số cetane cao của 85 – 96 làm bắt đầu cho động cơ diesel và xăng dầu do biến động cao và autoignition tại nhiệt độ thấp
- Dung môi này còn được ứng dụng trong quá trình sản xuất ra nhựa cellulose
Cảm ơn bạn đã đọc bài viết. Mong rằng với những chia sẻ của Kovacova qua bài viết này, đã giải đáp được thắc mắc cho bạn về tính chất hóa học của ete. Chúc bạn có một ngày tốt lành