Độ kiềm là gì? Nó có tác dụng gì đối với nước và được tính như thế nào? Đây là chủ đề mà nhiều người quan tâm. Nhất là những người yêu thích về hóa học. Bạn hãy cùng Kovacova tìm hiểu rõ hơn về chủ đề này trong bài viết dưới đây nhé!
1. Độ kiềm là gì? Độ kiềm trong nước là gì?
Độ kiềm là phép đo những chất kiềm hòa tan trong nước, độ kiềm của nước là số đo khả năng trung hòa axit của nước. Độ kiềm có 3 loại chính: Bicarbonate, carbonate, hydroxide
Độ kiềm tổng là tổng hàm lượng của những ion hydrocacbonat(HCO3-), cacbonat (CO32-), hydroxyl (OH-) và ion muối của những axit yếu khác (photphat, silicat, và những axit muối hữu cơ)
Độ kiềm của nước tự nhiên
Độ kiềm của nước thiên nhiên có độ PH<8,4 chính là lượng ion hydrocacbonat HCO3-, đôi khi cả hợp chất của các axit hữu cơ. Trong nước bị ô nhiễm hoặc ở hiện trạng kỵ khí, muối của những axit yếu như axit acetic, propionic và hydrogen sulfide cũng có khả năng tạo thành độ kiềm. Trong một số trường hợp khác, amoni hoặc các hydroxide cũng gây ra độ kiềm cho nước.Trong những điều kiện khăng khăng, những nguồn nước thiên nhiên có khả năng chứa một lượng đáng kể độ kiềm cacbonat và hydroxide. Điều kiện này thường diễn ra trong nguồn nước mặt có tảo tăng cường. Tảo sử dụng khí cacbonic dạng tự do và liên hợp trong nước và PH thường có giá trị 9 – 10.
Mặc dù rất nhiều chất gây nên độ kiềm trong nước nhưng một số đông độ kiềm của nước thiên nhiên do 3 chất gây ra theo thứ kiêu ngạo thuộc vào giá trị PH từ cao đến thấp: hydroxide (OH-), cacbonate (CO3-) và bicacbonate (HCO3-)
Độ kiềm của nước làm mềm
Độ kiềm của nước khi làm mềm bằng giải pháp trao đổi ion cũng được quyết định bằng lượng ion HCO3- đôi khi cả hợp chất của axit hữu cơ nếu nó tồn tại trong nước nguồn.
Đối với nước sau khi được xử lý làm mềm bằng biện pháp hóa học sử dụng vôi hoặc soda thường chứa cacbonat và hydroxide.
2. Công dụng của độ kiềm trong nước
Độ kiềm là một chỉ tiêu quan yếu trong xử lý nước. Độ kiềm của nước về nguyên tắc do muối của các axit yếu và những loai bazo mạnh gây ra và các chất này là dung dịch đệm để giữ PH không giảm nhiều khi đưa axit vào nước. do đó độ kiềm còn là số đo khả năng đệm của nước và được sử dụng lớn trong xử lý nước cấp cũng như xử lý nước thải.
Độ kiềm của nước tác động đến hiệu quả keo tụ
các hóa chất keo tụ được sử dụng để keo tụ nước và nước thải phản ứng với nước để tạo thành kết tủa hydroxide không hòa tan. Ion hydro giải phóng ra sẽ phản ứng với độ kiềm của nước. thành ra độ kiềm có tác dụng đệm cho PH tối ưu cho quá trình keo tụ. Độ kiềm phải ở mức đủ để trung hòa lượng axit được giải phóng ra từ chất keo tụ và hoàn tất quá trình keo tụ.
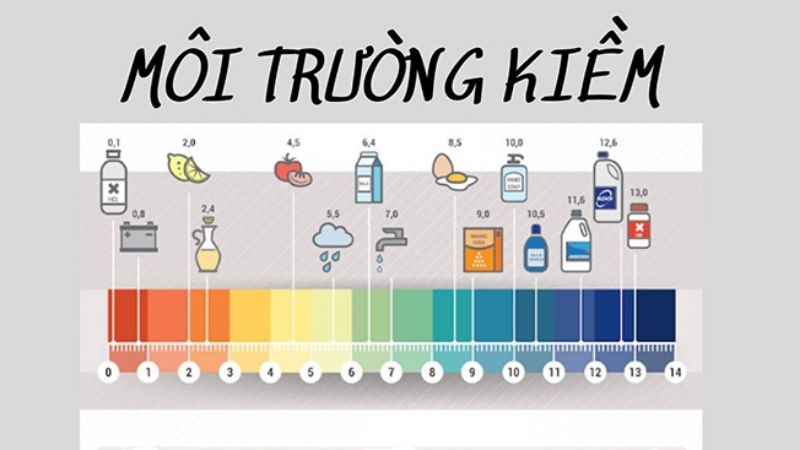
Làm mềm nước
Độ kiềm là thông số chính phải được xem xét đến trong việc tính toán mục tiêu về vôi và soda trong quá trình làm mềm nước. Độ kiềm của nước được làm mềm phải nằm trong giới hạn của tiêu chuẩn nước uống
Kiểm soát ăn mòn
Độ kiềm là tham số cấp thiết liên can đến việc kiểm soát quá trình ăn mòn. Đây là tham số cần nhận biết để tính toán chỉ số bão hòa Langelier
Khả năng đệm
Số đo độ kiềm được sử dụng như một tham số để đánh giá khả năng đệm của nước thải và bùn
Chất thải công nghiệp
Nhiều công ty cấm việc xả thải chất thải chứa độ kiềm hydroxide vào nguồn nước. Độ kiềm cũng như độ PH của nước là nhân tố quan yếu khi xác đinh khả năng xử lý sinh học của nước thải.
Chất lượng nước bể bơi
Đối với nước bể bơi, độ kiềm tổng của nước phải ở mức chuẩn 60 – 100 ppm. Độ kiềm của nước hồ bơi không đạt chuẩn sẽ khiến khó điều chỉnh độ PH có khả năng gây nên hàng loạt các câu hỏi khác như gây ngứa, bỏng rát, xót mắt, rêu tảo, nước hồ bơi bị đục.

Trên đây, Kovacova đã giải đáp cho bạn về chủ đề “Độ kiềm là gì? Những công dụng của độ kiềm trong nước”. Hy vọng những thông tin trên hữu ích với bạn. Cảm ơn bạn đã đọc bài viết của chúng tôi.
>>Xem thêm: vai trò của kali đối với cây trồng